 夜黎
夜黎本文章內容基於萊斯大學 OpenStax 的 Anatomy and Physiology 2e,由夜黎重新編輯。(根據本書前言中的創用 CC BY 4.0 聲明)
原文傳送門:<2> The Chemical Level of Organization — 2.5 Organic Compounds Essential to Human Functioning
索引傳送門:《解剖學和生理學2e》索引頁面
學習本章後,你將能夠:
- 確定對人體功能至關重要的四種有機分子
- 解釋有機化合物中,碳對共價鍵的親和力背後的化學原理
- 提供三種碳水化合物的例子,並確定碳水化合物在體內的主要功能
- 討論對人體功能很重要的四種脂質
- 描述蛋白質的結構,並討論它們對人類功能的重要性
- 識別核酸的組成部分,以及 DNA、RNA 和 ATP 在人類功能中的作用
前言
有機化合物通常由與氫(通常是氧)以及其他元素共價鍵合的碳原子團組成。 它們遍布世界各地,存在於土壤和海洋、商業產品以及人體的每個細胞中。 對人體結構和功能最重要的四種類型是碳水化合物〔carbohydrates〕、脂質〔lipids〕、蛋白質〔proteins〕和核酸〔nucleic acids〕。 在探索這些化合物之前,你需要首先了解碳的化學性質。
碳的化學
有機化合物之所以無處不在,是因為其碳核〔carbon core〕的化學性質。 回想一下,碳原子的價殼層中有四個電子,八位組規則〔octet rule〕規定原子傾向於這樣的方式反應,用八個電子完成其價電子層。 碳原子並不是通過捐贈或接受四個電子來完成其價殼層。 相反,它們很容易通過共價鍵共享電子。
通常,碳原子與其他碳原子共享,通常形成稱為碳骨架〔carbon skeleton〕的長碳鏈〔long carbon chain〕。 然而,當它們確實共享時,它們並不只彼此共享所有電子。 相反,碳原子傾向於與各種其他元素共享電子,其中之一總是氫。 碳和氫基團稱為碳氫化合物〔hydrocarbons〕。 如果你在本章的剩餘部分研究有機化合物的圖形,你將在化合物的一個區域中看到一些帶有碳氫化合物鏈的化合物。
許多組合可以填補碳的四個“空缺〔vacancies〕”。 碳可以與有機化合物的特定區域中的氧或氮或其他原子共享電子。 此外,碳原子鍵合的原子也可以是官能基〔functional group〕的一部分。 官能基是通過強共價鍵連接的一組原子,並且傾向於在化學反應中作為單個單元發揮作用。 你可以將官能基視為緊密結合的“派系〔cliques〕”,其成員不太可能分開。 五個官能基在人體生理學中很重要; 它們是羥基〔hydroxyl group〕、羧基〔carboxyl group〕、氨基〔amino group〕、甲基〔methyl group〕和磷酸基〔phosphate group〕(表 2.1)。
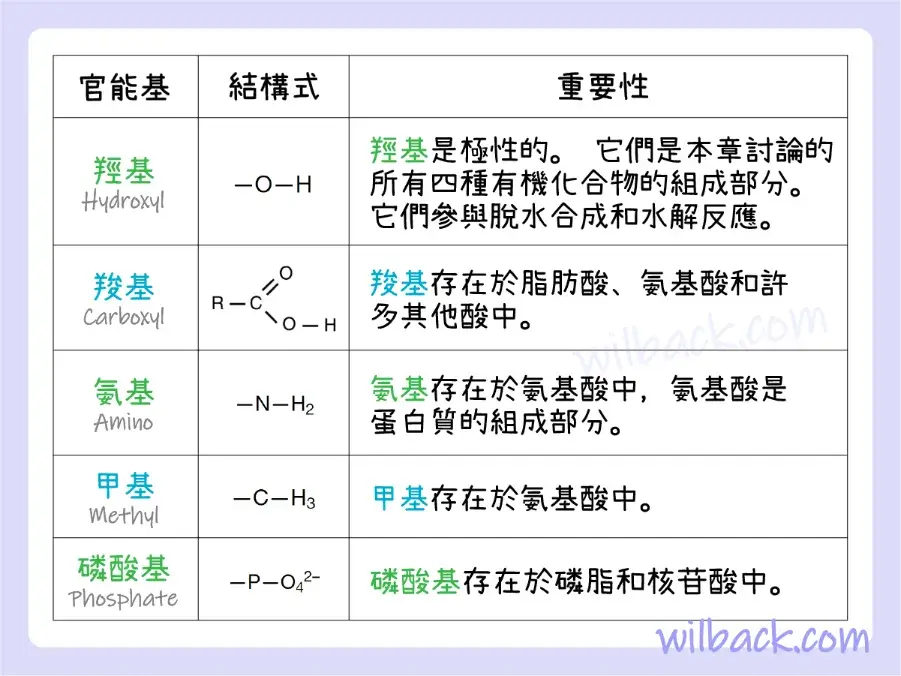

在人類生理學中重要的官能基
碳對共價鍵的親和力意味著許多不同且相對穩定的有機分子仍然很容易形成更大、更複雜的分子。 任何大分子都被稱為高分子〔macromolecule〕(macro-=“大”),本節中的有機化合物都符合這種描述。 然而,一些大分子是由稱為單體〔monomer〕的單個單元的多個“副本〔copies〕”組成(mono-=“一個”;-mer=“部分”)。 就像長項鍊上的珠子一樣,這些單體通過共價鍵連接形成長聚合物(poly-=“許多”)。 有機化合物中有許多單體和聚合物的例子。
單體通過脫水合成〔dehydration synthesis〕形成聚合物(見圖2.14)。 如前所述,該反應導致水分子的釋放。 每種單體都貢獻:一個給出一個氫原子,另一個給出一個羥基〔hydroxyl group〕。 聚合物通過水解〔hydrolysis〕分裂成單體(-lysis=“破裂〔rupture〕”)。 它們的單體之間的鍵通過提供一個水分子而被打破,水分子為一個單體提供一個氫原子,為另一個單體提供一個羥基。
碳水化合物
碳水化合物一詞的意思是“水合碳〔hydrated carbon〕”。 回想一下,詞根 Hydro- 表示水。 碳水化合物是由碳、氫和氧組成的分子; 在大多數碳水化合物中,氫和氧的相對比例與水中的2:1相同。 事實上,“通用〔generic〕”碳水化合物分子的化學式是 (CH2O)n 。
碳水化合物被稱為醣〔saccharides〕,這個詞的意思是“糖〔sugars〕”。 三種形式在身體中很重要。 單醣〔monosaccharides〕是碳水化合物的單體。 二糖〔disaccharides〕(di-=“兩個”)由兩個單體組成。 多醣〔polysaccharides〕是聚合物,可以由數百至數千個單體組成。
單醣
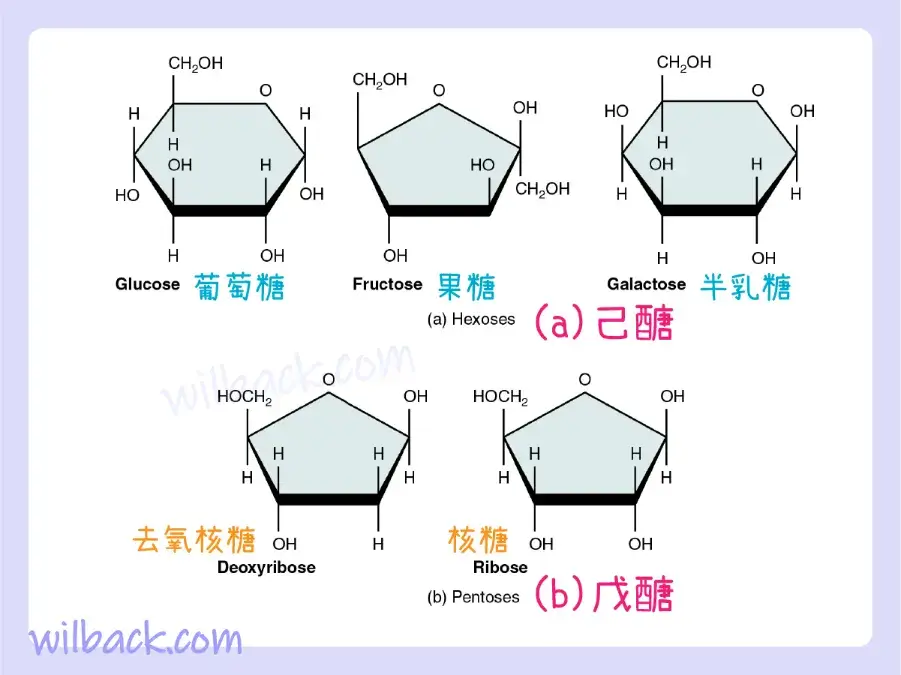
單醣〔monosaccharide〕是碳水化合物的單體。 五種單醣在體內很重要。 其中三種是己糖〔hexose sugars〕,之所以如此命名是因為它們各自含有六個碳原子。 它們是葡萄糖〔glucose〕、果糖〔fructose〕和半乳糖〔galactose〕,如圖 2.18a 所示。 剩下的單醣是兩個戊糖〔pentose sugars〕,每個都含有五個碳原子。 它們是核糖〔ribose〕和脫氧核糖〔deoxyribose〕,如圖2.18b所示。

二糖
二糖〔disaccharide〕是一對單醣。 二糖是通過脫水合成〔dehydration synthesis〕形成的,連接它們的鍵稱為糖苷鍵〔glycosidic bond〕(glyco–=“糖”)。 三種二糖(如圖 2.19 所示)對人類很重要。 這些是蔗糖〔sucrose〕,通常稱為食用糖〔table sugar〕; 乳糖〔lactose〕,或乳糖〔milk sugar〕; 和麥芽糖〔maltose〕,或麥芽糖〔malt sugar〕。 從它們的通用名稱中可以看出,你在飲食中消耗了它們; 但是,你的身體無法直接使用它們。 相反,在消化道中,它們通過水解分解成其成分單醣。
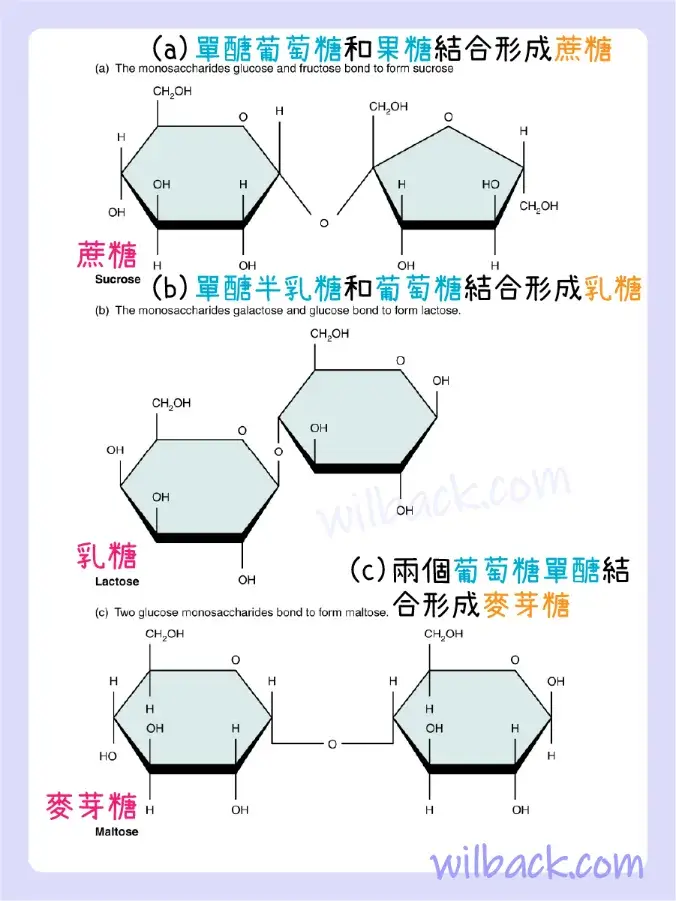

所有三種重要的二糖都是通過脫水合成形成的。
多醣
多醣〔polysaccharides〕可以含有幾個到一千個或更多個單醣。 其中三個對身體很重要(圖2.20):
- 澱粉〔starches〕是葡萄糖的聚合物。 它們以稱為直鏈澱粉〔amylose〕的長鍊或稱為支鏈澱粉〔amylopectin〕的支鏈形式存在,兩者都儲存在植物性食品中並且相對容易消化。
- 肝醣〔glycogen〕也是葡萄糖的聚合物,但它儲存在動物的組織中,尤其是肌肉和肝臟中。 它不被視為膳食碳水化合物,因為屠宰後動物組織中殘留的糖原很少; 然而,人體又將多餘的葡萄糖以糖原的形式儲存在肌肉和肝臟中。
- 纖維素〔cellulose〕是一種多醣,是綠色植物細胞壁的主要成分,是植物性食物的成分,被稱為“纖維”。 對於人類來說,纖維素/纖維〔cellulose/fiber〕是不可消化的; 然而,膳食纖維對健康有很多好處。 它可以幫助你感到飽足,從而減少食量,促進消化道健康,高纖維飲食被認為可以降低患心髒病和某些癌症的風險。
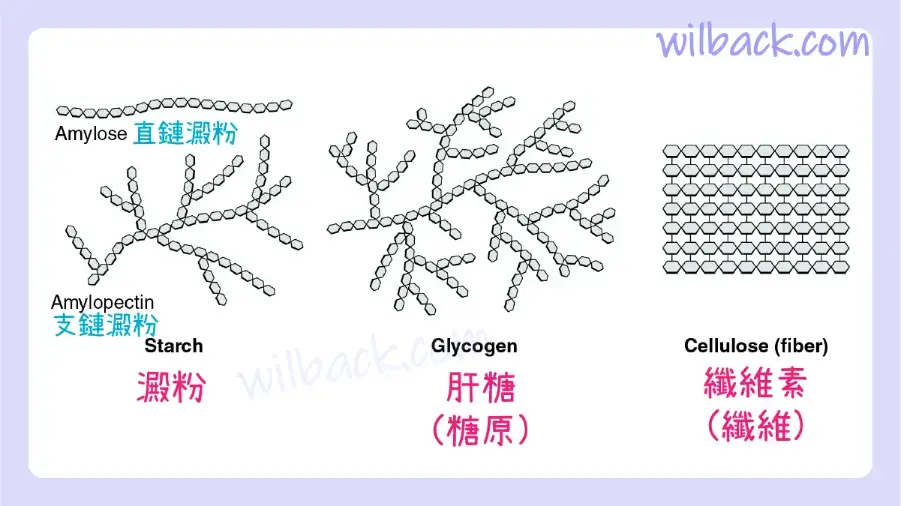

三種重要的多醣是澱粉、糖原和纖維。
碳水化合物的功能
身體從植物性食物中獲取碳水化合物。 儘管乳製品中含有乳糖,但穀物、水果、豆類和其他蔬菜提供了人類飲食中的大部分碳水化合物。
儘管大多數身體細胞可以分解其他有機化合物作為燃料,但所有身體細胞都可以使用葡萄糖。 而且,大腦、脊髓以及周圍神經系統中的神經細胞(神經元)以及紅血球只能使用葡萄糖作為燃料。 在葡萄糖分解為能量的過程中,產生了三磷酸腺苷分子,即 ATP。 三磷酸腺苷(ATP)〔adenosine triphosphate〕由核糖〔ribose suga〕、腺嘌呤鹼基〔adenine base〕和三個磷酸基〔phosphate groups〕組成。 當 ATP 的磷酸鍵〔phosphate bonds〕斷裂時,ATP 會釋放自由能,從而為細胞提供現成的能量。 有氧氣 (O2) 存在時比不使用氧氣的途徑中產生更多的 ATP。 將葡萄糖中的能量轉化為 ATP 中儲存的能量的總反應可以寫為:
C6H12O6 + 6 O2 → 6 CO2 + 6 H2O + ATP
除了作為重要的燃料來源外,碳水化合物在細胞結構中的含量也非常少。 例如,一些碳水化合物分子與蛋白質結合產生糖蛋白〔glycoproteins〕,而另一些則與脂質結合產生醣脂 〔glycolipids〕,這兩種分子都存在於包圍體細胞內容物的膜〔membrane〕中。
脂質
脂質〔lipid〕是主要由碳氫化合物組成的高度多樣化的化合物之一。 它們含有的少數氧原子通常位於分子的外圍。 它們的非極性碳氫化合物使所有脂質都具有疏水性。 在水中,脂質不會形成真正的溶液,但它們可能會形成乳液〔emulsion〕,這是指不能很好混合的溶液混合物的術語。
三酸甘油酯
三酸甘油酯〔triglyceride〕是最常見的膳食脂質之一,也是身體組織中含量最豐富的類型。 這種化合物通常被稱為脂肪,是由兩種類型的分子合成形成的(圖 2.21):
- 甘油三酯核心的甘油骨架由三個碳原子組成。
- 三個脂肪酸〔fatty acids〕,即兩端帶有羧基〔carboxyl group〕和甲基〔methyl group〕的長碳氫鏈,從甘油的每個碳上延伸出來。
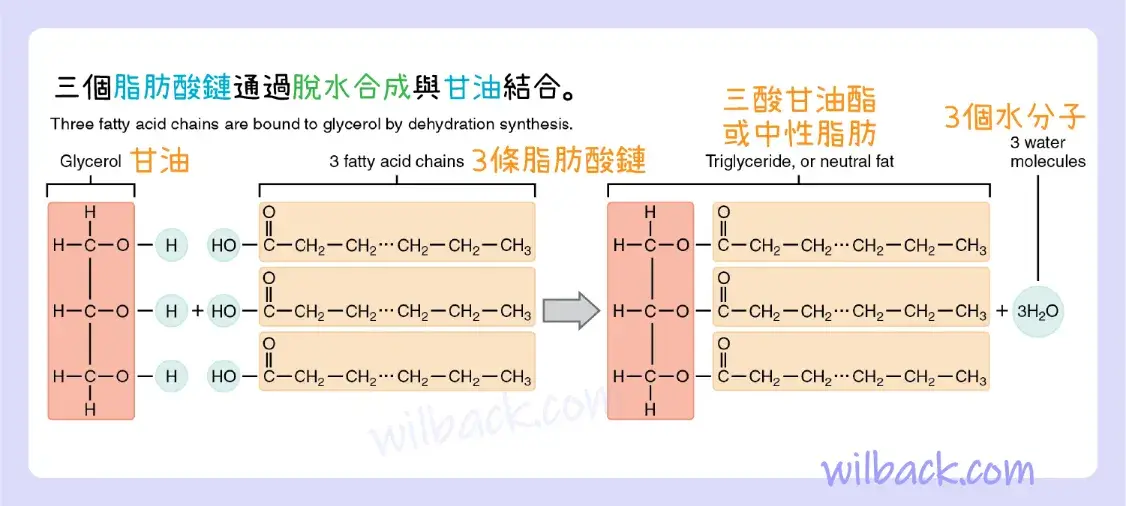

三酸甘油酯由甘油通過脫水合成與三個脂肪酸連接而成。 請注意,甘油放棄一個氫原子,脂肪酸上的羧基各自放棄一個羥基。
通過脫水合成形成三酸甘油酯。 甘油從每個鍵上的羥基中釋放出氫原子,並且每個脂肪酸鏈上的羧基釋放出羥基。 總共三個水分子由此被釋放。
沿其長度任何地方都沒有雙碳鍵並因此含有最大數量氫原子的脂肪酸鏈稱為飽和脂肪酸〔saturated fatty acids〕。 這些筆直的剛性鏈緊密地堆積在一起,在室溫下呈固態或半固態(圖 2.22a)。 黃油和豬油就是例子,牛排或你體內的脂肪也是如此。 相比之下,具有一個雙碳鍵的脂肪酸在該鍵處扭結(圖 2.22b)。 因此,這些單不飽和脂肪酸〔monounsaturated fatty acids〕無法緊密地堆積在一起,並且在室溫下呈液態。 多不飽和脂肪酸〔polyunsaturated fatty acids〕含有兩個或多個雙碳鍵,在室溫下也是液體。 植物油(例如橄欖油)通常含有單不飽和脂肪酸和多不飽和脂肪酸。
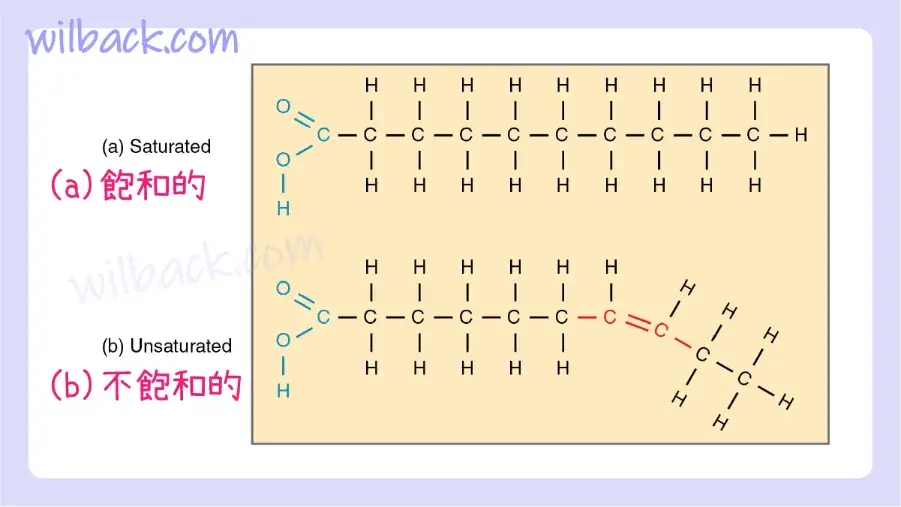

脂肪酸的飽和度影響其形狀。 (a) 飽和脂肪酸鍊是直鏈。 (b) 不飽和脂肪酸鏈扭結。
然而,富含飽和脂肪酸的飲食會增加患心髒病的風險,富含不飽和脂肪酸的飲食被認為可以降低風險。 對於鮭魚等冷水魚中的 omega-3 不飽和脂肪酸來說尤其如此。 這些脂肪酸的第一個雙碳鍵位於甲基的第三個碳氫化合物處(稱為分子的omega末端)。
最後,一些加工食品(包括一些棒狀和桶狀人造黃油〔stick and tub margarines〕)中發現的反式脂肪酸〔trans fatty acids〕被認為比飽和脂肪酸對心臟和血管的危害更大。 反式脂肪是由不飽和脂肪酸(例如玉米油)經過化學處理產生部分氫化脂肪〔partially hydrogenated fats〕而產生的。
作為一個整體,三酸甘油酯是身體的主要燃料來源。 當你休息或睡眠時,用於維持生命的大部分能量來自儲存在脂肪〔fat (adipose)〕組織中的三酸甘油酯。 三酸甘油酯還可以為長時間、緩慢的體力活動(例如園藝或徒步旅行)提供能量,並為劇烈的體力活動提供適度比例的能量。 膳食脂肪還有助於非極性脂溶性維生素A、D、E 和K 的吸收和運輸。此外,儲存的身體脂肪可以保護和緩衝身體的骨骼和內臟,並起到隔熱作用以保持身體熱量。
脂肪酸也是醣脂〔glycolipids〕的組成部分,醣脂是細胞膜中發現的醣脂肪化合物。 脂蛋白〔lipoproteins〕是疏水性三酸甘油酯包裝在蛋白質包膜中以便在體液中運輸的化合物。
磷脂
顧名思義,磷脂〔phospholipid〕是脂質的甘油成分和磷分子之間的鍵。 事實上,磷脂的結構與三酸甘油酯相似。 然而,磷脂不是由三個脂肪酸組成,而是由二酸甘油酯〔diglyceride〕(一種僅具有兩個脂肪酸鏈的甘油)生成(圖 2.23)。 甘油上的第三個結合位點被磷酸基〔phosphate group〕佔據,磷酸基團又連接到分子的極性“頭部”區域。 回想一下,三酸甘油酯是非極性且疏水的。 這對於磷脂化合物的脂肪酸部分仍然成立。 然而,磷脂的頭部在磷酸基團以及氮原子上含有電荷。 這些電荷使磷脂頭具有親水性。 因此,磷脂具有疏水性尾部(含有中性脂肪酸)和親水性頭部(含有帶電磷酸基團和氮原子)。
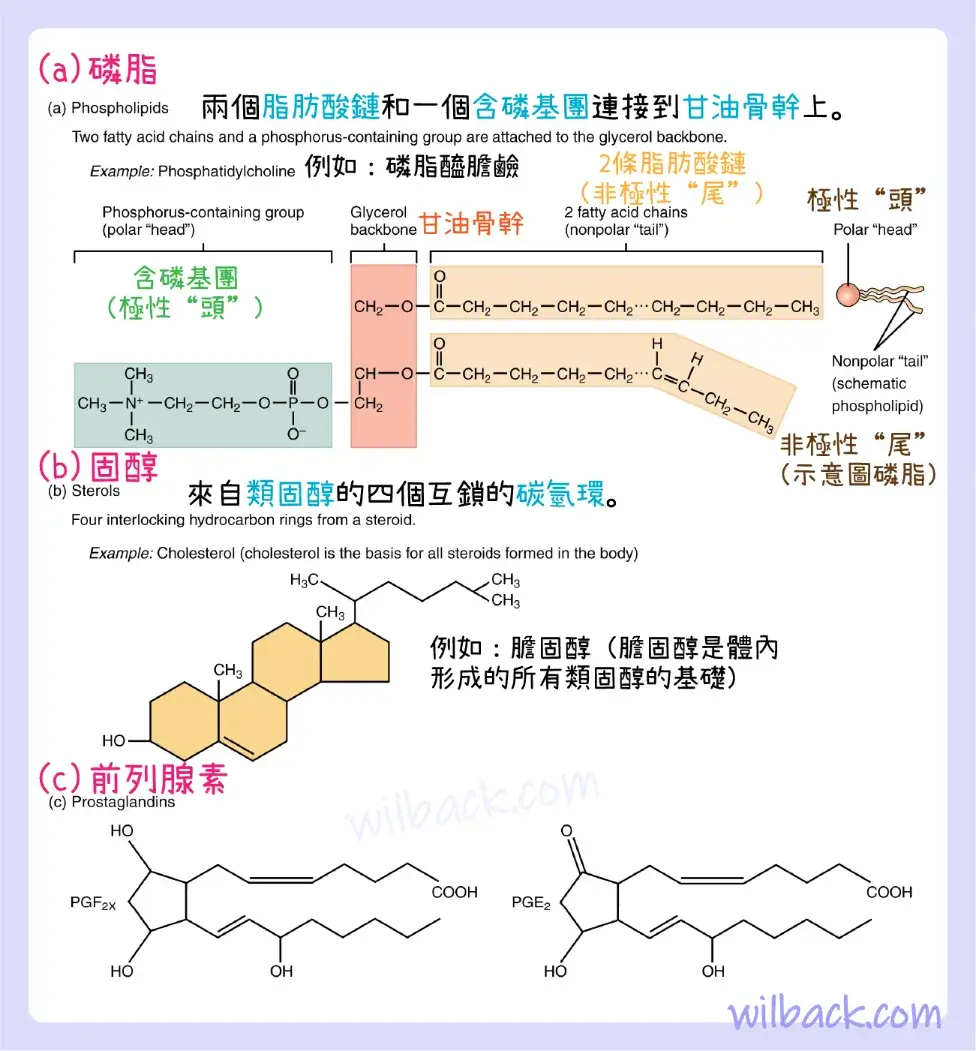

(a) 磷脂由兩種脂肪酸、甘油和一個磷酸基團組成。 (b) 固醇[Sterols]是環狀脂質。 這裡顯示的是膽固醇。 (c) 前列腺素衍生自不飽和脂肪酸。 前列腺素 E2 (PGE2) 包含羥基和羧基。
類固醇
類固醇〔steroid〕化合物(稱為固醇〔sterol〕)以一組與各種其他原子和分子鍵合的四個碳氫環為基礎(見圖 2.23b)。 雖然植物和動物都會合成固醇,但對人體結構和功能最重要貢獻的類型是膽固醇,它由人類和動物的肝臟合成,也存在於大多數動物性食品中。 與其他脂質一樣,膽固醇的碳氫化合物使其具有疏水性。 然而,它具有親水性的極性羥基頭。 膽固醇是膽汁酸〔bile acids〕的重要組成部分,膽汁酸是有助於乳化膳食脂肪的化合物。 事實上,詞根“chole-”指的是膽汁。 膽固醇也是許多激素的組成部分,身體釋放信號分子來調節遠處的過程。 最後,與磷脂一樣,膽固醇分子也存在於細胞膜中,其疏水性和親水性區域有助於調節物質進出細胞的流動。
前列腺素
與激素一樣,前列腺素〔prostaglandin〕是一組信號分子之一,但前列腺素源自不飽和脂肪酸(見圖 2.23c)。 魚中的 omega-3 脂肪酸有益的原因之一是它們可以刺激某些前列腺素的產生,這些前列腺素有助於調節血壓和炎症,從而降低患心髒病的風險。 前列腺素還能使神經對疼痛敏感。 一類名為非類固醇消炎藥物 (NSAID) 的止痛藥物通過減少前列腺素的作用發揮作用。
蛋白質
你可能會將蛋白質與肌肉組織聯繫起來,但事實上,蛋白質是所有組織和器官的關鍵組成部分。 蛋白質〔protein〕是由通過肽鍵〔peptide bonds〕連接的氨基酸組成的有機分子。 蛋白質包括皮膚表皮中保護皮下組織的角蛋白〔keratin〕、皮膚真皮、骨骼以及覆蓋大腦和脊髓的腦膜中的膠原蛋白。 蛋白質也是人體許多功能性化學物質的組成部分,包括消化道中的消化酶、抗體、神經元用來與其他細胞交流的神經遞質,以及調節某些身體功能的肽類激素(例如生長激素)。 雖然碳水化合物和脂質由碳氫化合物和氧組成,但所有蛋白質除了碳、氫和氧外,還含有氮 (N),並且許多蛋白質還含有硫 (S)。
蛋白質的微觀結構
蛋白質是由稱為氨基酸的含氮單體組成的聚合物。 氨基酸〔amino acids〕是由氨基和羧基以及可變側鏈組成的分子。 僅僅 20 種不同的氨基酸就構成了對人體結構和功能至關重要的幾乎所有數千種不同蛋白質。 身體蛋白質含有這 20 種氨基酸單體中幾十到幾百個的獨特組合。 所有 20 種氨基酸都具有相似的結構(圖 2.24)。 所有這些都由一個中心碳原子組成,其中鍵合有以下物質:
- 一個氫原子
- 鹼性〔alkaline (basic)〕氨基 NH2(見表2.1)
- 酸性羧基 COOH(見表2.1)
- 變量組
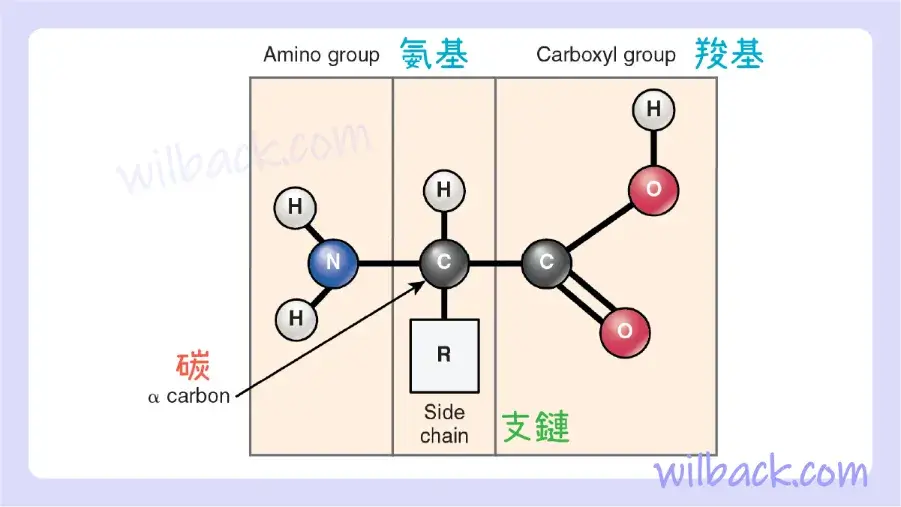

請注意,所有氨基酸都含有酸(羧基)和鹼(氨基)(amine=“含氮〔nitrogen-containing〕”)。 因此,它們是極好的緩衝劑,幫助身體調節酸鹼平衡。 20 種氨基酸的區別在於它們的可變基團〔variable group〕,稱為支鏈〔side chain〕或殘基〔R-group〕。 該基團的大小可以不同,可以是極性的或非極性的,從而賦予每種氨基酸其獨特的特性。 例如,兩種氨基酸(半胱氨酸〔cysteine〕和蛋氨酸〔methionine〕)的支鏈含有硫。 硫不易參與氫鍵,而所有其他氨基酸則參與。 這種變異影響含有半胱氨酸和蛋氨酸的蛋白質的組裝方式。
氨基酸通過脫水合成結合形成蛋白質聚合物(圖 2.25)。 將氨基酸結合在一起的獨特鍵稱為肽鍵。 肽鍵〔peptide bond〕是兩個氨基酸之間通過脫水合成形成的共價鍵。 事實上,肽是一種非常短的氨基酸鏈。 含有少於約100個氨基酸的鏈通常被稱為多肽〔polypeptides〕而不是蛋白質。
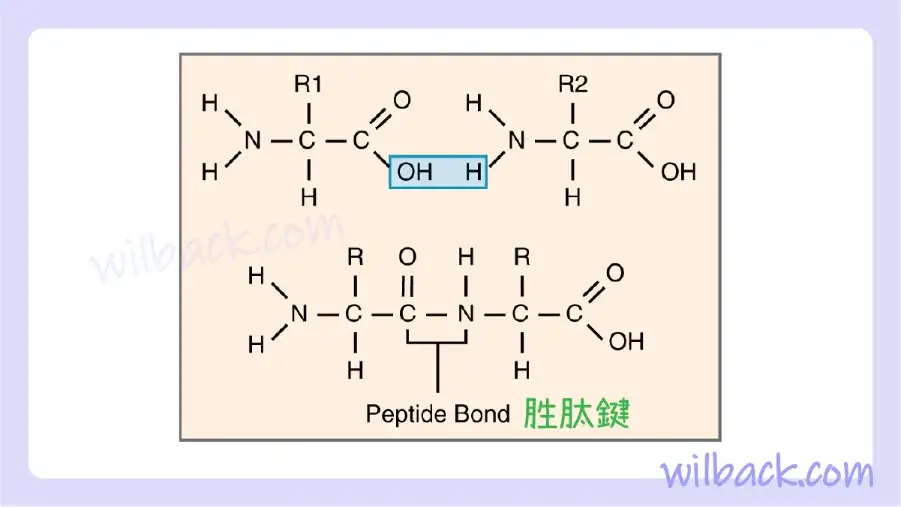

不同的氨基酸通過脫水合成結合在一起形成肽、多肽或蛋白質。 氨基酸之間的鍵是肽鍵,R1和R2可以是相同或不同的側鏈。
身體能夠從其他分子的成分合成大部分氨基酸; 然而,九種元素無法合成,必須通過飲食攝入。 這些被稱為必需氨基酸〔essential amino acids〕。
可用於蛋白質構建的游離氨基酸被認為駐留在細胞內的氨基酸池〔amino acid pool〕中。 細胞內的結構在組裝蛋白質時使用這些氨基酸。 然而,如果氨基酸池中沒有足夠數量的特定必需氨基酸,則含有該氨基酸的蛋白質的合成可能會減慢甚至停止。
蛋白質的形狀
正如叉子不能用來喝湯,勺子不能用來叉肉一樣,蛋白質的形狀對其功能至關重要。 蛋白質的形狀從根本上來說是由構成蛋白質的氨基酸序列決定的(圖 2.26a)。 該序列稱為蛋白質的一級結構。
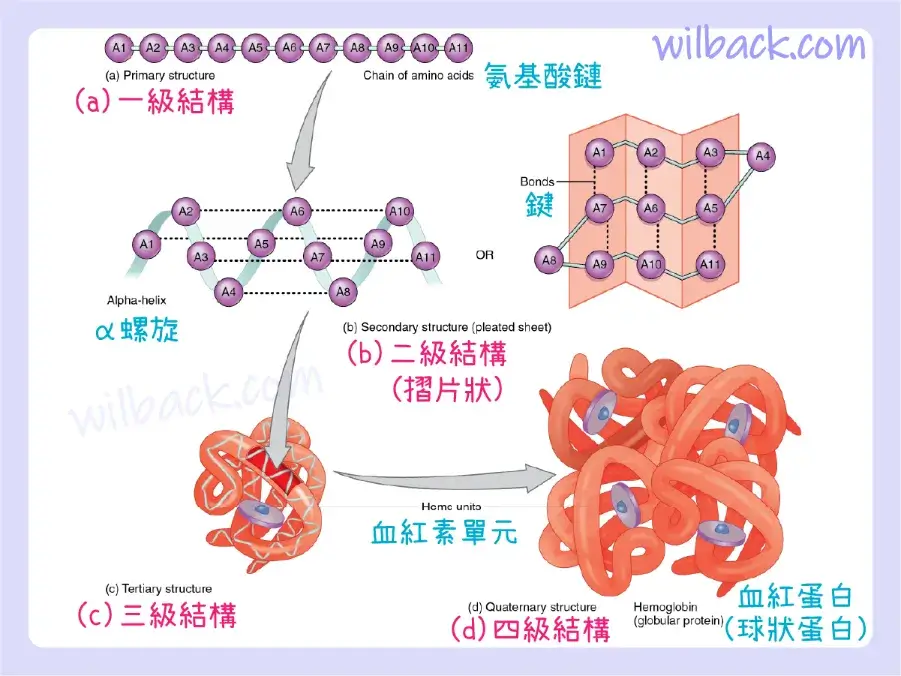

儘管一些多肽以直鏈形式存在,但大多數都扭曲或折疊成更複雜的二級結構,這些結構是在多肽不同區域具有不同特性的氨基酸之間發生鍵合時形成的。 最常見的二級結構是稱為α螺旋〔alpha-helix〕的螺旋。 如果你拿一根繩子,簡單地把它扭成螺旋形,它就無法保持形狀。 同樣,如果沒有氫鍵的幫助,一條氨基酸鏈就無法保持穩定的螺旋形狀,氫鍵會在同一鏈的不同區域之間形成橋樑(見圖 2.26b)。 不太常見的是,多肽鏈可以形成β摺片〔beta-pleated sheet〕,其中氫鍵在自身折疊的單個多肽的不同區域之間或在兩個或更多個相鄰多肽鏈之間形成橋。
蛋白質的二級結構進一步折疊成緊湊的三維形狀,稱為蛋白質的三級結構(見圖2.26c)。 在這種構型中,主鏈中距離很遠的氨基酸可以通過氫鍵變得非常接近,或者在含有半胱氨酸的蛋白質中通過雙硫鍵變得非常接近。 雙硫鍵〔disulfide bonds〕是多肽中硫原子之間的共價鍵。 通常,兩個或多個單獨的多肽結合形成更大的具有四級結構的蛋白質(見圖 2.26d)。 形成四級結構的多肽亞基可以相同或不同。 例如,血紅蛋白(紅血球中發現的蛋白質)由四個三級多肽組成,其中兩個稱為α鏈,兩個稱為β鏈。
當它們暴露於極熱、酸、鹼和某些其他物質時,蛋白質會變性。 變性〔denaturation〕是通過物理或化學手段改變分子結構。 變性的蛋白質失去其功能形狀,不再能夠執行其工作。 蛋白質變性的一個常見例子是添加酸性檸檬汁後牛奶凝結。
蛋白質的形狀對其功能的貢獻怎麼誇大都不過分。 例如,構成肌肉組織的蛋白質鏈的細長形狀對於其收縮(縮短)和放鬆(延長)的能力至關重要。 另一個例子,骨頭含有一種叫做膠原蛋白的長絲蛋白質,它充當骨礦物質沉積在其上的支架。 這些細長的蛋白質稱為纖維蛋白,堅固耐用,通常具有疏水性。
相比之下,球狀蛋白是球體〔globes〕或球體〔spheres〕,往往具有高反應性並且是親水性的。 紅血球中的血紅蛋白就是一個例子(見圖 2.26d); 然而,球狀蛋白在全身大量存在,在大多數身體功能中發揮著關鍵作用。 早先作為蛋白質催化劑引入的酶就是這樣的例子。 下一節將仔細研究酶的作用。
蛋白質具有酶的功能
如果你嘗試打字,並且每次按下筆記本電腦上的按鍵時,都會延遲六到七分鐘才能得到回應,那麼你可能會購買一台新筆記本電腦。 同樣的道理,如果沒有酶來催化化學反應,人體就會失去功能。 它之所以起作用只是因為酶起作用。
酶促反應〔enzymatic reactions〕(由酶催化的化學反應)在底物與酶結合時開始。 受質〔substrate〕是酶促反應中的反應物。 這發生在被稱為活性位點〔active sites〕的酶區域(圖 2.27)。 任何給定的酶僅催化一種類型的化學反應。 這種特性稱為特異性〔specificity〕,是由於具有特定形狀和電荷的受質只能與該底物對應的活性位點結合。
由於酶與其受質之間的這種類似拼圖遊戲的匹配,酶以其特異性而聞名。 事實上,當酶與其受質結合時,酶結構會發生輕微變化,以找到過渡狀態〔transition state〕(受質和產物之間的結構中間體)和活性位點之間的最佳配合,就像橡膠手套成型一樣一隻手插入其中。 這種在受質存在下的活性位點修飾以及同時形成的過渡態被稱為誘導擬合〔induced fit〕。 總體而言,每種受質以及每種化學反應都有一種專門匹配的酶; 然而,也有一定的靈活性。 一些酶能夠作用於幾種不同的結構相關受質。
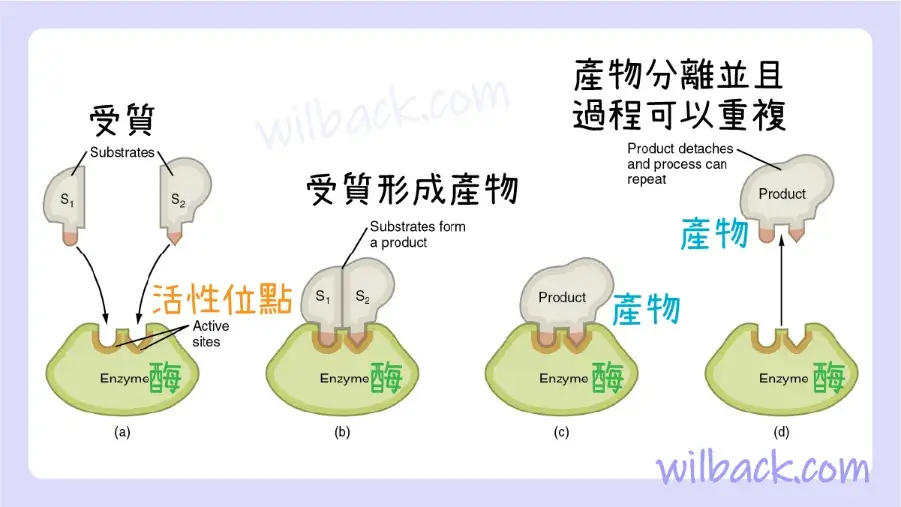

受質的結合產生酶-受質複合物。 酶加速化學反應的部分原因可能是酶-受質複合物經歷了一系列暫時且可逆的變化,導致受質以最佳位置彼此定向,以促進它們的相互作用。 這促進了反應速度的提高。 然後酶釋放產物,並恢復其原始形狀。 然後,酶可以自由地再次參與該過程,並且只要受質剩餘,酶就會繼續參與該過程。
蛋白質的其他功能
蛋白質棒〔bars〕、蛋白質粉〔powders〕和蛋白質奶昔〔shakes〕的廣告都說蛋白質對於構建、修復和維持肌肉組織很重要,但事實是蛋白質對從皮膚到腦細胞的所有身體組織都有貢獻。 此外,某些蛋白質還充當激素、化學信使,幫助調節身體功能,例如,生長激素對骨骼生長等很重要。
如前所述,鹼性和酸性成分使蛋白質能夠充當維持酸鹼平衡的緩衝劑,但它們也有助於調節液體—電解質平衡〔electrolyte balance〕。 蛋白質吸引液體,「血液」、「細胞」和「細胞之間的空間」中蛋白質的健康濃度有助於確保這些不同“隔室〔compartments〕”中液體的平衡。 此外,細胞膜中的蛋白質有助於將電解質輸送進出細胞,使這些離子保持健康的平衡。 像脂質一樣,蛋白質可以與碳水化合物結合。 因此,它們可以產生糖蛋白〔glycoproteins〕或蛋白聚醣〔proteoglycans〕,這兩種物質在體內都有許多功能。
當碳水化合物和脂肪攝入不足,並且糖原和脂肪組織的儲存耗盡時,身體可以利用蛋白質作為能量。 然而,由於除了功能組織外沒有蛋白質的儲存場所,利用蛋白質作為能量會導致組織分解,導致身體浪費。
核苷酸
對人體結構和功能很重要的第四種有機化合物是核苷酸(圖 2.28)。 核苷酸〔nucleotide〕是由三個亞基〔subunits〕組成的一類有機化合物之一:
- 一個或多個磷酸基團〔phosphate groups〕
- 戊糖〔pentose sugar〕:脫氧核糖〔deoxyribose〕或核糖〔ribose〕
- 含氮鹼基〔nitrogen-containing base〕:腺嘌呤〔adenine〕、胞嘧啶〔cytosine〕、鳥嘌呤〔guanine〕、胸腺嘧啶〔thymine〕或尿嘧啶〔uracil〕
核苷酸可以組裝成核酸(DNA或RNA)或能量化合物三磷酸腺苷〔adenosine triphosphate〕。
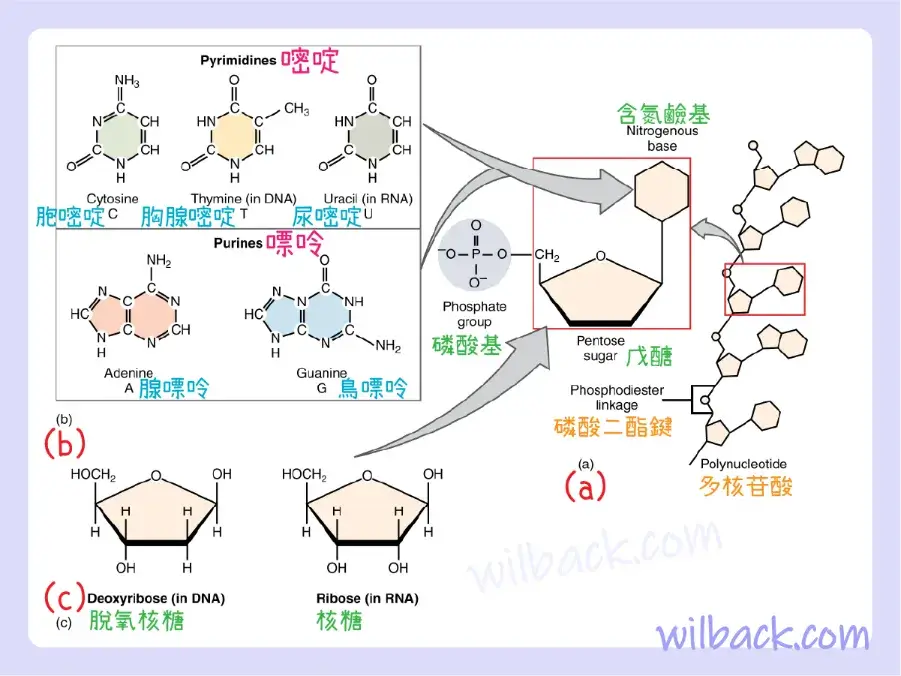

(a) 所有核苷酸的組成部分是一個或多個磷酸基團、戊糖和含氮鹼基。 (b) 核苷酸的含氮鹼基。 (c) DNA 和 RNA 的兩種戊糖。
核酸
核酸的戊醣類型不同。 脫氧核糖核酸(DNA)〔deoxyribonucleic acid〕是儲存遺傳信息的核苷酸。 DNA 含有脫氧核糖〔deoxyribose〕(之所以這麼說是因為它比核糖少 1 個氧原子)加上 1 個磷酸基團和 1 個含氮鹼基。 DNA 鹼基的“選擇”是腺嘌呤〔adenine〕、胞嘧啶〔cytosine〕、鳥嘌呤〔guanine〕和胸腺嘧啶〔thymine〕。 核糖核酸(RNA)〔ribonucleic acid〕是一種含有核糖的核苷酸,有助於將遺傳密碼表現為蛋白質。 RNA含有核糖、一個磷酸基團和一個含氮鹼基,但 RNA 的鹼基“選擇”是腺嘌呤〔adenine〕、胞嘧啶〔cytosine〕、鳥嘌呤〔guanine〕和尿嘧啶〔uracil〕。
含氮鹼基腺嘌呤〔adenine〕和鳥嘌呤〔guanine〕被歸類為嘌呤。 嘌呤〔purines〕是一種具有雙環結構的含氮分子,其中含有多個氮原子。 鹼基胞嘧啶〔cytosine〕、胸腺嘧啶〔thymine〕(僅存在於 DNA 中)和尿嘧啶〔uracil〕(僅存在於 RNA 中)是嘧啶。嘧啶〔pyramidines〕是具有單環結構的含氮鹼基。
一種核酸單體的戊糖與另一種核酸單體的磷酸基團之間脫水合成形成的鍵形成“骨架〔backbone〕”,各組分的含氮鹼基從中突出。 在 DNA 中,兩個這樣的主鏈通過氫鍵連接在其突出的鹼基上。 這些扭曲形成稱為雙螺旋的形狀(圖 2.29)。 DNA 鏈內的含氮鹼基序列形成基因,這些基因充當指導細胞將氨基酸組裝成蛋白質的分子密碼。 人類的 DNA 中有近 22,000 個基因,被鎖定在每個細胞核內的 46 條染色體中(除了在發育過程中失去細胞核的紅血球)。 這些基因攜帶著構建身體的遺傳密碼,除了同卵雙胞胎之外,每個人都是獨一無二的。
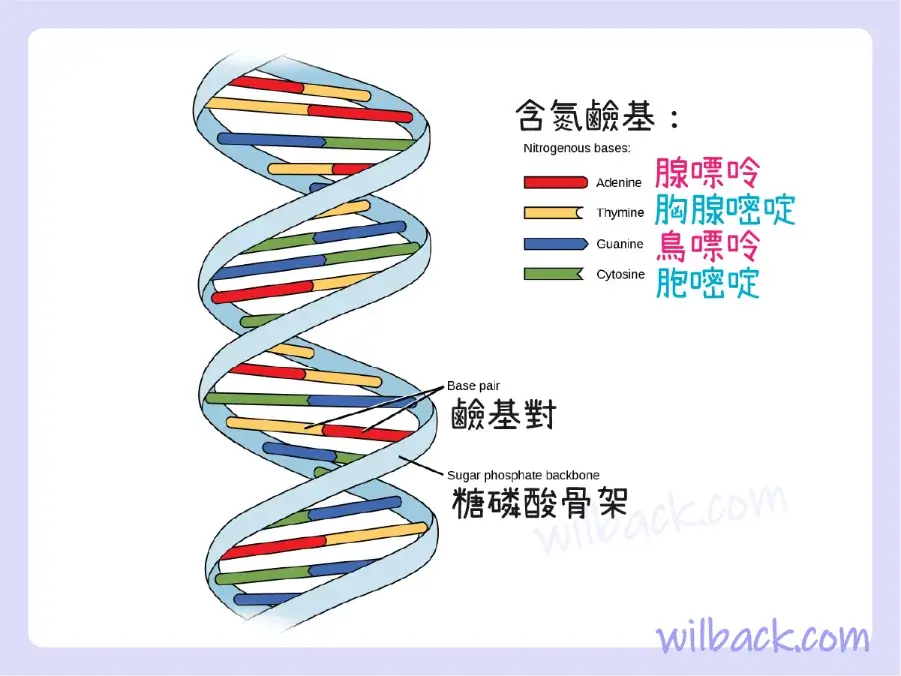

在 DNA 雙螺旋中,兩條鏈通過組成核苷酸的鹼基之間的氫鍵連接。
相比之下,RNA 由單鏈糖磷酸骨架〔sugar-phosphate backbone〕組成,上面散佈著鹼基。 信使 RNA (mRNA) 在蛋白質合成過程中產生,將 DNA 的遺傳指令攜帶到細胞質中的細胞蛋白質製造工廠(核醣體〔ribosomes〕)。
三磷酸腺苷
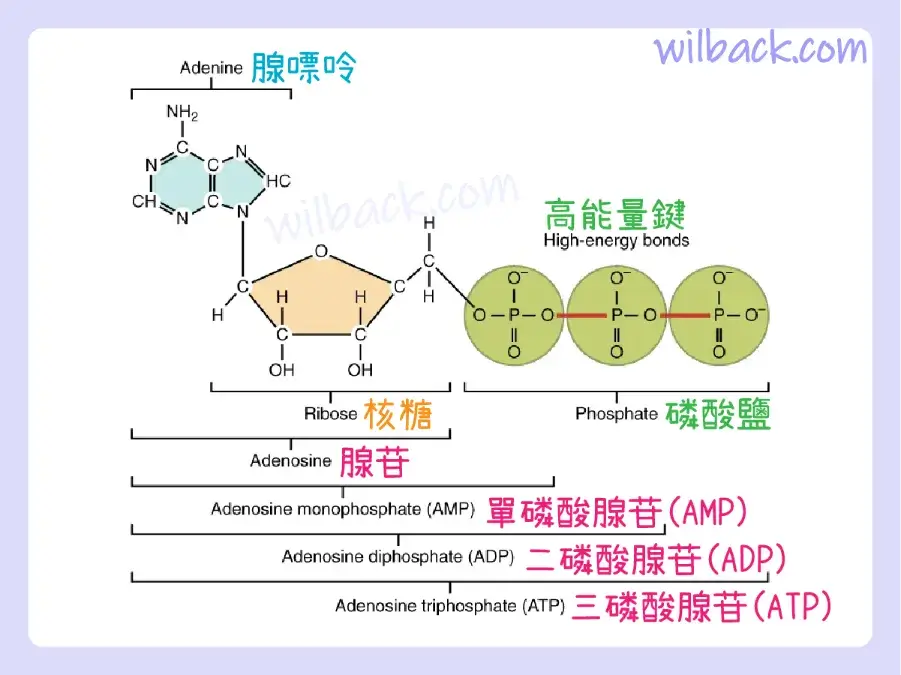
核苷酸三磷酸腺苷 (ATP) 〔nucleotide adenosine triphosphate〕由核糖、腺嘌呤鹼基〔adenine base〕和三個磷酸基團組成〔phosphate groups〕(圖 2.30)。 ATP 被歸類為高能化合物,因為連接其三個磷酸鹽的兩個共價鍵儲存了大量的位能。 在體內,這些高能鍵釋放的能量有助於促進身體的活動,從肌肉收縮到物質進出細胞的運輸,再到合成代謝化學反應。

當磷酸基團從 ATP 上裂解時,產物是二磷酸腺苷 (ADP) 和無機磷酸鹽 (Pi)。 該水解反應可寫為:
ATP + H2O → ADP + Pi + energy
去除第二個磷酸鹽留下單磷酸腺苷〔adenosine monophosphate〕和兩個磷酸基團。 同樣,這些反應也釋放了儲存在磷酸鹽-磷酸鹽鍵中的能量。 當 ADP 發生磷酸化時,它們也是可逆的。 磷酸化〔phosphorylation〕是在有機化合物上添加磷酸基,在這種情況下會產生 ATP。 在這種情況下,水解過程中釋放的相同水平的能量必須重新投入到脫水合成中。
細胞還可以將磷酸基從 ATP 轉移到另一種有機化合物。 例如,當葡萄糖首次進入細胞時,磷酸基從 ATP 轉移,形成磷酸葡萄糖 (C6H12O6-P) 和 ADP。 一旦葡萄糖以這種方式磷酸化,它就可以作為糖原儲存或代謝為即時能量。
更新紀錄
2023/09/11 發佈本文


評論